Đề kiểm tra học kì I môn Hóa học Lớp 10 - Trường THPT Krông Ana (Có đáp án)
Bạn đang xem tài liệu "Đề kiểm tra học kì I môn Hóa học Lớp 10 - Trường THPT Krông Ana (Có đáp án)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Đề kiểm tra học kì I môn Hóa học Lớp 10 - Trường THPT Krông Ana (Có đáp án)
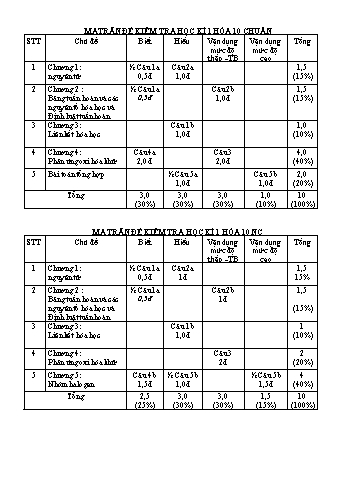
MA TRÂN ĐỀ KIỂM TRA HỌC KÌ 1 HÓA 10 CHUẨN STT Chủ đề Biết Hiểu Vận dụng Vận dụng Tổng mức độ mức độ thấp -TB cao 1 Chương 1: ½ Câu 1a Câu 2a 1,5 nguyên tử 0,5đ 1,0đ (15%) 2 Chương 2 : ½ Câu 1a Câu 2b 1,5 Bảng tuần hoàn và các 0,5đ 1,0đ (15%) nguyên tố hóa học và Định luật tuần hoàn 3 Chương 3: Câu 1b 1,0 Liên kết hóa học 1,0đ (10%) 4 Chương 4: Câu 4a Câu 3 4,0 Phản ứng oxi hóa khử 2,0 đ 2,0đ (40%) 5 Bài toán tổng hợp ½ Câu 5a Câu 5b 2,0 1,0đ 1,0đ (20%) Tổng 3,0 3,0 3,0 1,0 10 (30%) (30%) (30%) (10%) (100%) MA TRÂN ĐỀ KIỂM TRA HỌC KÌ 1 HÓA 10 NC STT Chủ đề Biết Hiểu Vận dụng Vận dụng Tổng mức độ mức độ thấp -TB cao 1 Chương 1: ½ Câu 1a Câu 2a 1,5 nguyên tử 0,5đ 1đ 15% 2 Chương 2 : ½ Câu 1a Câu 2b 1,5 Bảng tuần hoàn và các 0,5đ 1đ nguyên tố hóa học và (15%) Định luật tuần hoàn 3 Chương 3: Câu 1b 1 Liên kết hóa học 1,0đ (10%) 4 Chương 4: Câu 3 2 Phản ứng oxi hóa khử 2đ (20%) 5 Chương 5: Câu 4b ½ Câu 5b ½ Câu 5b 4 Nhóm halogen 1,5đ 1,0đ 1,5đ (40%) Tổng 2,5 3,0 3,0 1,5 10 (25%) (30%) (30%) (15%) (100%) . .. .. .. . .. .. .. . .. .. .. . .. .. .. . .. .. .. . .. .. .. . .. .. .. . .. .. .. . .. .. .. . .. .. .. .. . PHẦN Viết đúng mỗi pt 1 đ, viết 2 trong 3 pt sau: 2 pt 2 điểm RIÊNG Fe + 2HCl FeCl2 + H2. Câu MnO2 + 4HCl MnCl2 + Cl2 + 2H2O 4A(2 đ) CuO + H2 Cu + H2O Câu 5A 4,35 0,25 điểm Số mol MnO2 = = 0,05 (mol) (2 đ) 87 0,5 đ a. MnO2 + 4 HCl MnCl2 + Cl2 + 2H2O. 0,05 mol 0,2mol 0,05 mol 0,25 đ 0,5 đ b. Thể tích Cl2 là V = 0,05 x 22,4 = 1,12 lit c. Khối lượng HCl phản ứng là m = 0,2x36,5 = 7,3g 0,25 đ Khối lượng dd HCl là: mdd = 20.1,25 = 25g Nồng độ phần trăm dung dịch HCl là 7,3 C% = x100% = 29,2% gam 0,25 đ 25 Nâng (1) 2KMnO4 + 16HCl 2KCl + 2MnCl2 + 5Cl2 + 8H2O Mỗi pt as cao (2) Cl2 + H2 2HCl 0,25đ 4B(1,5đ) (3) 2HCl + Fe FeCl2 + H2 (4) 2FeCl2 + Cl2 2FeCl3 (5) FeCl3 + 3NaOH Fe(OH)3 + 3NaCl (6) NaCl + AgNO3 AgCl + NaNO3 Câu 5B a. MnO2 + 4HCl → MnCl2 + Cl2 + 2 H2O Viết đúng 2 pt (2,5đ) 0,4 0,4 0,5đ Cl2 + 2NaOH → NaCl + NaClO + H2O 0,4 0,8 0,4 0,4 Tính VCl2 V Cl2 = 0,4.22,4 = 8,96 lit 0,5 đ b. n MnO2 = 34,8: 87= 0,4 mol n NaOH = 1 mol dd A : NaCl : 0,4 mol NaClO : 0,4 mol 0,25 đ NaOH dư : 0,2 mol Khối lượng dung dịch sau phản ứng = 200 + 0,4.71 = 228,4 0,5đ gam 0,4.58,5 0,25 đ C% NaCl = .100 % = 10,25% 228,4 0,4.74,5 C% NaClO = .100 % = 13,00% 228,4 0,25đ 0,2.40 C% NaOH = .100% = 3,50% 0,25 đ 228,4
File đính kèm:
 de_kiem_tra_hoc_ki_i_mon_hoa_hoc_lop_10_truong_thpt_krong_an.doc
de_kiem_tra_hoc_ki_i_mon_hoa_hoc_lop_10_truong_thpt_krong_an.doc

