Tài liệu Hướng dẫn tự học môn Hóa học 11 (Lần 5)
Bạn đang xem tài liệu "Tài liệu Hướng dẫn tự học môn Hóa học 11 (Lần 5)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Tài liệu Hướng dẫn tự học môn Hóa học 11 (Lần 5)
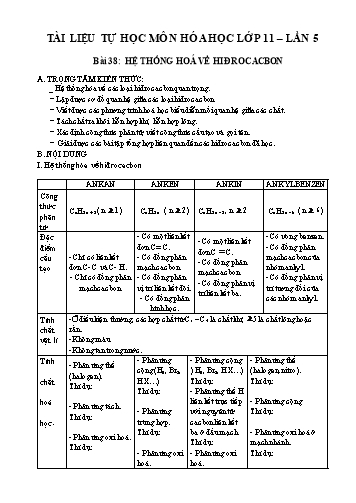
TÀI LIỆU TỰ HỌC MƠN HĨA HỌC LỚP 11 – LẦN 5 Bài 38: HỆ THỐNG HỐ VỀ HIĐROCACBON A. TRỌNG TÂM KIẾN THỨC: _ Hệ thống hĩa về các loại hiđrocacbon quan trọng. Lập được sơ đồ quan hệ giữa các loại hiđrocacbon. Viết được các phương trình hố học biểu diễn mối quan hệ giữa các chất. Tách chất ra khỏi hỗn hợp khí, hỗn hợp lỏng. Xác định cơng thức phân tử, viết cơng thức cấu tạo và gọi tên. Giải được các bài tập tổng hợp liên quan đến các hiđrocacbon đã học. B. NỘI DUNG I. Hệ thống hĩa về hiđrocacbon ANKAN ANKEN ANKIN ANKYLBENZEN Cơng thức C H ( n 1) C H ( n 2) C H , n 2 C H ( n 6) phân n 2n + 2 n 2n n 2n - 2 n 2n - 6 tử Đặc - Cĩ một liên kết - Cĩ vịng benzen. - Cĩ một liên kết điểm đơn C= C. - Cĩ đồng phân đơn C C. cấu - Chỉ cĩ liên kết - Cĩ đồng phân mạch cacbon của - Cĩ đồng phân tạo đơn C- C và C- H. mạch cacbon. nhĩm ankyl. mạch cacbon. - Chỉ cĩ đồng phân - Cĩ đồng phân - Cĩ đồng phân vị - Cĩ đồng phân vị mạch cacbon. vị trí liên kết đơi. trí tương đối của trí liên kết ba. - Cĩ đồng phân các nhĩm ankyl. hình học. Tính -Ở điều kiện thường, các hợp chất từ C1 – C4 là chất khí; 5 là chất lỏng hoặc chất rắn. vật lí -Khơng màu. -Khơng tan trong nước. Tính - Phản ứng - Phản ứng cộng - Phản ứng thế - Phản ứng thế cộng (H , Br , ) H , Br , HX) (halogen, nitro). (halogen). 2 2 2 2 chất HX) Thí dụ: Thí dụ: Thí dụ: Thí dụ: - Phản ứng thế H hố liên kết trực tiếp - Phản ứng cộng - Phản ứng tách. - Phản ứng với nguyên tử Thí dụ: Thí dụ: học. trùng hợp. cacbon liên kết Thí dụ: ba ở đầu mạch. - Phản ứng oxi hố ở - Phản ứng oxi hố. Thí dụ: mạch nhánh. Thí dụ: - Phản ứng oxi - Phản ứng oxi Thí dụ: hố. hố. CHƯƠNG 8: DẪN XUẤT HALOGEN ANCOL – PHENOL Bài 40: ANCOL A. TRỌNG TÂM KIẾN THỨC: Định nghĩa, phân loại ancol. Cơng thức chung, đặc điểm cấu tạo phân tử, đồng phân, danh pháp (gốc chức và thay thế). Tính chất vật lí : Nhiệt độ sơi, độ tan trong nước ; Liên kết hiđro. Tính chất hố học : Phản ứng của nhĩm OH (thế H, thế OH), phản ứng tách nước tạo thành anken hoặc ete, phản ứng oxi hố ancol bậc I, bậc II thành anđehit, xeton ; Phản ứng cháy. Tính chất riêng của glixerol (phản ứng với Cu(OH)2). B. NỘI DUNG I. ĐINH NGHĨA, PHÂN LOẠI: 1. Định nghĩa: Ancol là những hợp chất hữu cơ trong phân tử cĩ nhĩm hiđroxyl –OH liên kết trực tiếp với nguyên tử cacbon no.* Nguyên tử cacbon no là nguyên tử cacbon chỉ tạo liên kết đơn với nguyên tử khác Ví dụ: CH3OH, CH3CH2OH CH2 = CH- CH2 – OH 2. Phân loại: CƠ SỞ PHÂN LOẠI Số lượng nhĩm -OH Một nhĩm OH Nhiều nhĩm OH No , mạch a) Ancol no, đơn chức, e) Ancol no, mạch hở, đa hở mạch hở. chức CnH2n+1OH CnH2n+2-x(OH)x khơng no, b) Ancol khơng no, đơn Gốc hiđrocacbon mạch hở chức, mạch hở(1lk đơi) ( hở, vịng) CnH2n-1OH Thơm c) Ancol thơm, đơn chức. No (vịng) d) Ancol vịng no, đơn chức. Trong số các ancol trên, cĩ: * Ancol bậc 1: là ancol cĩ nhĩm -OH liên kết với cacbon bậc 1. * Ancol bậc 2: là ancol cĩ nhĩm -OH liên kết với cacbon bậc 2. Bậc ancol * Ancol bậc 3: là ancol cĩ nhĩm -OH liên kết với cacbon bậc 3. * Khơng cĩ ancol bậc 4. II . ĐỒNG PHÂN, DANH PHÁP: 1. Đồng phân: Cĩ 3 loại: 1) Khái niệm về liên kết hiđro. - Liên kết giữa nguyên tử H mang một phần điện tích dương của nhĩm –OH này khi ở gần nguyên tử O mang một phần điện tích âm của nhĩm –OH kia tạo thành một liên kết yếu gọi là liên kết hiđro: Thí dụ: - Liên kết hiđro giữa các phân tử ancol: O - H O - H O - H O - H R R R R 2) Ảnh hưởng của liên kết hiđro đến tính chất vật lí.( của ancol) - Tan nhiều trong nước. - Cĩ nhiệt độ sơi cao hơn các hiđrocacbon cĩ cùng M với rượu. VI. TÍNH CHẤT HỐ HỌC: - Do phân cực của các liên kết các phản ứng hố học của ancol xảy ra chủ yếu ở nhĩm chức OH: 1. Phản ứng thế H của nhĩm OH: a) Tính chất chung của ancol: - Tác dụng với kim loại kiềm ( Na, K) Tổng quát: 1 CnH2n + 1OH +NaCnH2n + 1ONa+ H2 2 - Các ancol + NaOH hầu như khơng phản ứng. b) Tính chất đặc trưng của glixerol: Dùng phản ứng này để phân biệt ancol đơn chức với ancol đa chức (cĩ nhĩm OH liền kề). 2C3H5 (OH)3 + Cu(OH)2 [C3H5 (OH)2O]2Cu + 2H2O Đồng (II) glixerat (Màu xanh ) 2. Phản ứng thế nhĩm OH: a) Phản ứng với axit vơ cơ: to TQ: R-OH + HA R –A + H2O to Ví dụ: C2H5OH + HBr C2H5 –Br + H2O b) Phản ứng với ancol ( tạo ete) H2SO4 đặc , 1400 C TQ: R -OH + H -O-R’ R – O – R’ + H2O Thí dụ: o H2SO4dac ,140 C C2H5OH + C2H5OH C2H5OC2H5 + H2O 3. Phản ứng tách nước: Từ một phân tử rượu (tạo anken) H SO đ ặc CH - CH 2 4 2 2 CH 2 = CH 2 + H O 170 0C 2 H OH etilen ancol etylic Đối với các ancol no, đơn chức, mạch hở (đk tương tự) H2SO4 đặc , 1700C CnH2n +1OH CnH2n + H2O Câu 4: Oxi hĩa ancol nào sau đây khơng tạo anđehit ? A. CH3OH. B. (CH3)2CHCH2OH. C. C2H5CH2OH D. CH3CH(OH)CH3. Câu 5: Viết các đồng phân và gọi tên ancol của hợp chất cĩ CTPT C4H10O Câu 6: Phân biệt các chất: etanol, glixerol, hex-1-en .......................................................................................... Bài 41: PHENOL A. TRỌNG TÂM KIẾN THỨC: Khái niệm phenol. Tính chất vật lí : Trạng thái, nhiệt độ sơi, nhiệt độ nĩng chảy, tính tan. Tính chất hố học : Tác dụng với natri, natri hiđroxit, nước brom. Ứng dụng của phenol. Khái niệm về ảnh hưởng qua lại giữa các nguyên tử trong phân tử hợp chất hữu cơ. B. NỘI DUNG I. Định nghĩa, phân loại: a) Thí dụ: OH OH CH 2 - OH CH 3 (A ) (B) (C) Phenol 2-m etylphenol ancol benzylic (phenyl m etanol) Phenol ancol thơm Phenol là những hợp chất hữu cơ trong phân tử cĩ nhĩm –OH liên kết trực tiếp với nguyên tử cacbon trong vịng benzen. - Phenol đơn giản: C6H5-OH. II. PHENOL: 1. Cấu tạo: - CTPT: C6H6O ( M =94) - CTCT: C6H5 –OH Hay: H O Bài tập vận dụng Câu 1: Phenol khơng phản ứng với chất nào sau đây ? A. Na. B. NaOH. C. NaHCO3. D. Br2. Câu 2: Phản ứng tạo kết tủa trắng của phenol với dung dịch Br2 chứng tỏ rằng A. Phenol cĩ nguyên tử hiđro linh động. B. Phenol cĩ tính axit. C. ảnh hưởng của nhĩm –OH đến gốc –C6H5 trong phân tử phenol D. ảnh hưởng của gốc –C6H5 đến nhĩm –OH trong phân tử phenol Câu 3: Để nhận biết ba lọ mất nhãn: phenol, stiren, ancol benzylic, người ta dùng một thuốc thử duy nhất là: A. Na B. Dung dịch NaOH C. Nước brom D. Ca(OH)2 Câu 4: Viết ptpư xảy ra (nếu cĩ) giữa ancol etylic, phenol với các chất sau : Na, NaOH, nước brơm, dd HNO3. Câu 5: Hồn thành dãy chuyển hĩa sau bằng các pt hĩa học : a. metan --> axetilen --> etilen --> etanol --> axit axetic. b. benzen --> brombenzen --> natriphenolat--> phenol-->2,4,6-tribromphenol. Câu 6: Cho hỗn hợp gồm etanol và phenol tác dụng với Na (dư) thu được 3,36 lít (đktc) khí H2 . Nếu cho hh trên tác dụng với dd nước brơm vừa đủ thu được 19,86 gam kết tủa trắng . a. Viết phản ứng xảy ra. b. Tính %(m) của mỗi chất ban đầu ? Câu 7: Cho 14,0 gam hỗn hợp A gồm ancol etylic, phenol tác dụng với natri dư thì thu được 2,24 lít khí hidro(đkc). a. Viết các phương trình phản ứng hĩa học xảy ra b. Tính thành phần phần trăm khối lượng từng chất trong A c. Cho 14,0 gam hỗn hợp A tác dụng với dung dịch HNO3( đủ) thì thu được bao nhiêu gam axit picric (2,4,6-trinitrophenol)
File đính kèm:
 tai_lieu_huong_dan_tu_hoc_mon_hoa_hoc_11_lan_5.doc
tai_lieu_huong_dan_tu_hoc_mon_hoa_hoc_11_lan_5.doc

